انرژي هاي يونش بالاتر
با اندکي مطالعه راجع به انرژي يونش و تشکيل يون هاي مختلف عناصر، متوجه مي شويد که سديم، منيزيم و آلومينيوم يون هاي Na+ و Mg2+ و Al3+ تشکيل مي دهند. اما آيا تا کنون از خود پرسيده ايد که چرا سديم، يون هاي Na2+ يا حتي Na3+ تشکيل نمي دهد؟
جواب اين سؤال مي تواند از انرژي دومين، سومين و ... يونش عناصر به دست آيد. به عنوان مثال، انرژي اولين يونش سديم، انرژي لازم براي برداشتن يک الکترون از يک اتم سديم خنثي است:
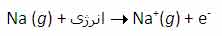
انرژي دومين يونش سديم، انرژي لازم براي برداشتن يک الکترون ديگر از يون Na+ در حالت گازي است که يک يونNa2+تشکيل مي دهد:
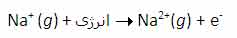
سومين انرژي يونش سديم نيز به همين ترتيب است:
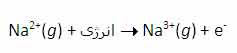
بنابراين انرژي لازم براي تشکيل يون Na3+ در فاز گازي، جمع انرژي هاي يونش اول، دوم و سوم اين عنصر است.
براي کندن يک الکترون از اتم سديم و تشکيل يون Na+ با آرايش الکتروني لايه پر، انرژي چندان زيادي لازم نيست اما وقتي يک بار اين اتفاق افتاد، براي برداشتن دومين الکترون از سديم تقريباً بايد 10 برابر انرژي يونش اوليه، انرژي صرف شود تا آرايش لايه پر Na+ شکسته شود و Na2+ تشکيل شود. به دليل اين که انرژي زيادي براي برداشتن دومين الکترون سديم در هر واکنش شيميايي لازم است، سديم مي تواند با عناصر ديگر طوري واکنش دهد که ترکيباتي شامل يون هاي Na+ تشکيل دهد نه يون هاي Na2+ يا Na3+.
اولين، دومين، سومين و چهارمين انرژي يونش سديم، منيزيوم و آلومينيوم (KJ/mol)
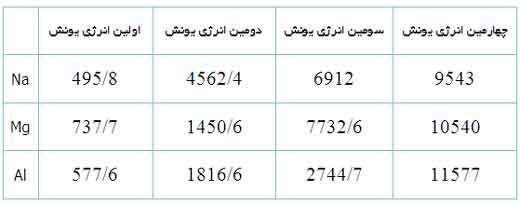
به دليل اين منيزيوم، يک پروتون بيش تر از سديم دارد، اولين انرژي يونش آن بيش تر است تا الکترون ها در اوربيتال 3s نگه دارد:
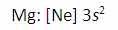
دومين انرژي يونش منيزيوم بزرگ تر از انرژي اولين يونش آن است زيرا هميشه برداشتن يک الکترون از يوني با بار مثبت، انرژي بيش تري مي گيرد تا بخواهيم همين اکترون را از يک اتم خنثي برداريم. سومين انرژي يونش منيزيوم خيلي زياد است زيرا Mg2+ آرايش پايدار و لايه پر دارد.
همين وضعيت راجع به آلومينيوم وجود دارد که اولين انرژي يونش آن از منيزيوم کم تر است. انرژي دومين و سومين يونش آلومينيوم از انرژي اولين يونش آن بزرگ تر است. اگرچه برداشتن سه الکترون از اتم آلومينيوم براي تشکيل يون Al3+مقدار انرژي زيادي لازم دارد اما انرژي لازم براي شکستن آرايش الکتروني پايدار يون Al3+ يک مقدار نجومي و عظيم است! بنابراين اشتباه است که به دنبال يون Al4+ به عنوان محصول يک واکنش شيميايي باشيم.
مسابقه وبلاگ برتر ماه
نظرات شما عزیزان:
برچسبها:






 آمار
وب سایت:
آمار
وب سایت:

